【今回はうちの吉田稔Dr.が書いてくれました。非常に実用的!ぜひ使ってください】
Generalistのための心房細動マネージメント:超基本その2
前回は0〜2は診断・緊急対応・原因精査に関してまとめました。
今回は、AFの治療に関してこの回はまとめました。詳細は、新・総合診療医学病院総合診療医学編第3版の『心房細動』を参照にしてください。
- 脳梗塞リスクの評価と治療の必要性、出血リスク評価、抗凝固薬の選択
3-1. 脳梗塞リスクの評価と治療の必要性
脳梗塞リスクを評価するにあたり、まず弁膜症性AFかどうかを評価する。ここでいう弁膜症性とは、僧帽弁狭窄症と人工弁置換後をさす[1]。弁膜症性AFでは塞栓症のリスクが高く、他のリスクに関わらずDOAC(direct oral anticoagulant:直接作用型経口抗凝固薬)ではなく、ワルファリンの投与を行う[1]。
非弁膜症性AFの脳梗塞リスクの評価には、CHADS2スコア・CHA2DS2-VAScスコアが用いられている(図1)。CHA2DS2-VAScスコアはより低リスク群を捉えることができるスコアである。我が国の心房細動治療ガイドライン(2013年改訂版)[1]ではCHADS2スコアですら十分に広まっていないことや簡便性を考慮し、CHADS2スコアを中心に足りない部分を追加する形で作成されている(図2)。CHADS2スコアが2点以上であれば、脳梗塞の予防効果が出血リスク(日本人のワルファリン投与中の頭蓋内出血発症率0.6〜1.0%/年 [1])を上回るため、積極的に抗凝固療法を行うべきである。

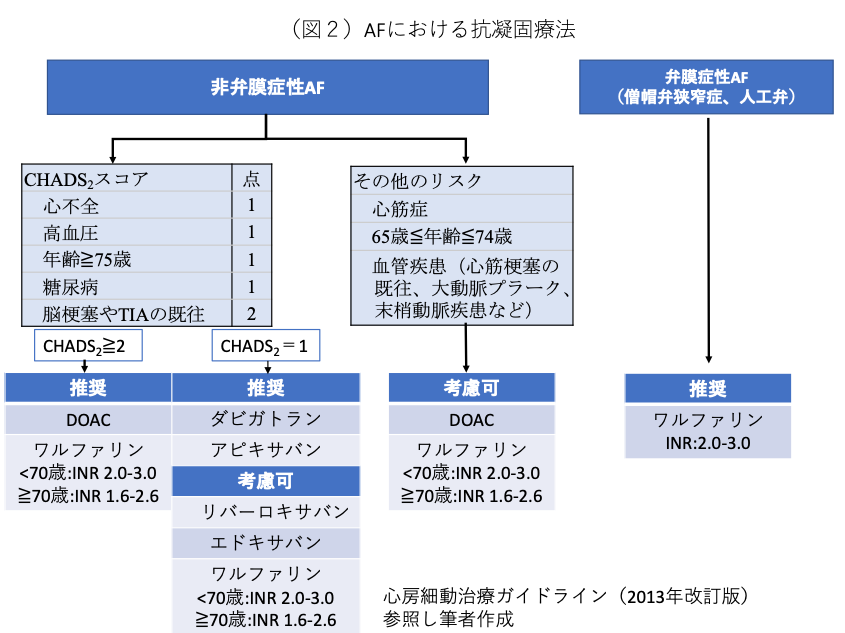
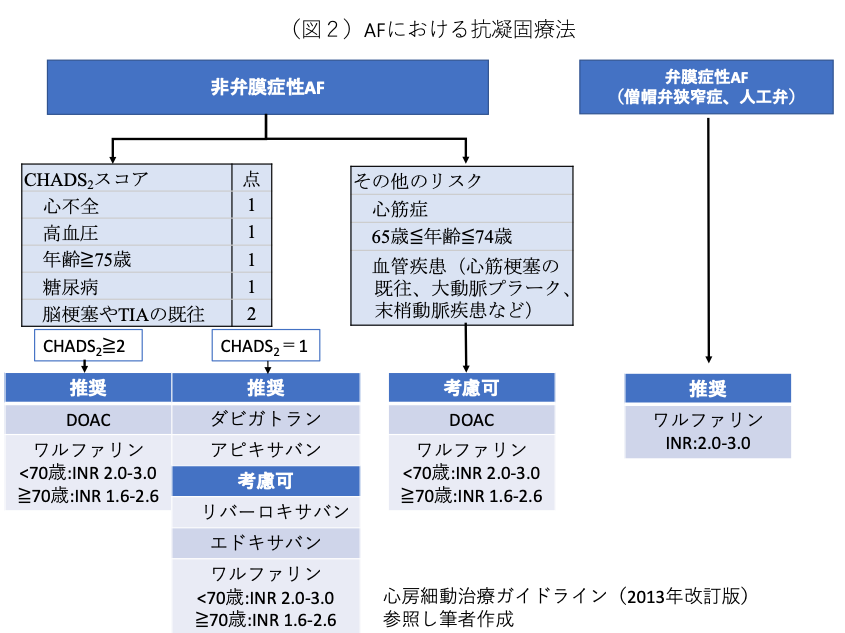
3-2. 出血リスクの評価
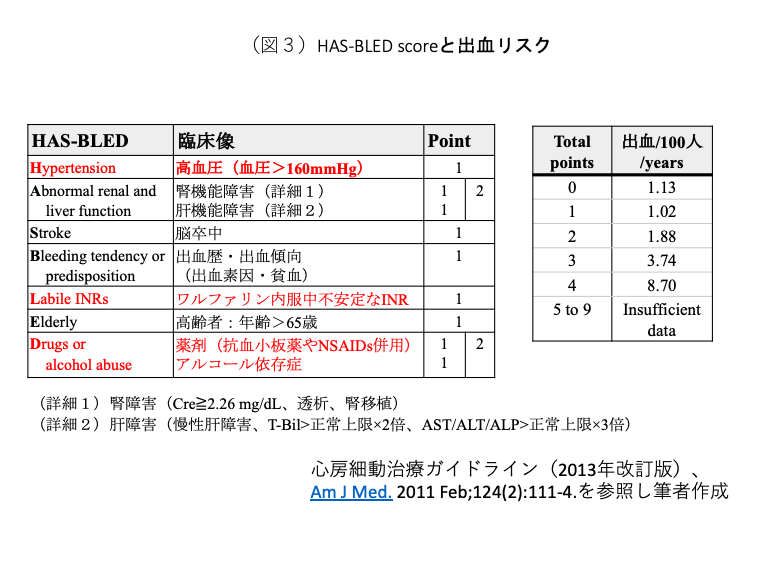
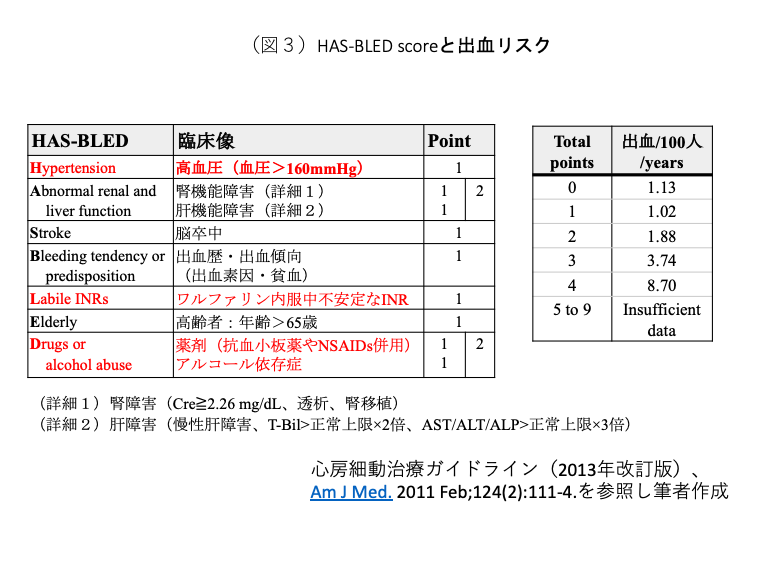
出血リスクの評価にはHAS-BLEDスコアが用いられるが有用性は十分ではない[2]。出血リスクを認識し、治療可能な因子をコントロールすることが重要である(図3の赤字はコントロール可能な因子)。血圧≦160 mmHgにコントロール(目標血圧<130 mmHg[3])、PT-INRが不安定な場合は適応があればワルファリンをDOACへの変更、不要な抗血小板薬・非ステロイド性抗炎症薬(NSAIDs)の中止、節酒・禁煙などの生活指導を行うことが重要である。
3-3. 抗凝固薬の選択
非弁膜症性AFでは、DOACは薬物間で差はあるが、ワルファリンと同等かそれ以上の効果・副作用予防効果を示している。腎機能、年齢、体重、嗜好(納豆・青汁など)、薬の自己負担額や併用薬を考慮して選択する。弁膜症性AFではワルファリンよりも有効性・安全性共に劣るためDOACは用いず、ワルファリンを選択する。
- レートコントロールの目的と方法
4-1.レートコントロールの目的[4]
・頻脈による血行動態不安定化を避ける・症状の改善
・頻脈誘発性心筋症を避ける
頻脈性AFによる血行動態の不安定化の病態生理は以下である。AFにより心房収縮が喪失する。洞調律時の心房収縮は血液の左室充満に重要な役割を果たしており、1回拍出量の約20-25%と言われている[5]。それに加えて、頻脈により拡張期が短縮し左室充満が減少する。その結果として、1回拍出量・心拍出量・冠動脈灌流の低下をきたし、血行動態の不安定化が起きる。HR>130 bpmを超えると心機能が低下する頻脈誘発性心筋症を起こす可能性がある[1]。
4-2. レートコントロールの方法
①左室機能(EF)≧40%:非ジヒドロピリジン系Ca拮抗薬(ベラパミル、ジルチアゼム)、β遮断薬どちらでも可。
②EF<40%・心不全の症状あり:β遮断薬を少量から慎重投与。ジギタリスも選択肢の一つ。血行動態が不安定・薬剤を併用してもレートコントロールできない場合はアミオダロンを考慮(非ジヒドロピリジン系Ca-blockerは陰性変力作用があるため避ける[2, 4])
- リズムコントロール 目的・方法
5.1 リズムコントロールの目的
電気的、薬理学的、いずれの除細動でも洞調律に回復・維持できれば、症状の改善、心房収縮による血液の左室充満の増加が期待できる。一方、基礎疾患としての心不全合併の有無に関わらず、薬理学的除細動によるリズムコントロールはレートコントロールと比べて、生命予後や心血管イベントの発生率に差を認めなかったという報告がある[2, 4]。心房細動に伴う自覚症状が主な適応であるが、その他、電気的、薬理学的除細動の適応となる因子は、若年、初発、レートコントロールが困難な場合、頻脈誘発性心筋症、患者の嗜好などがある[2]。
5.2 除細動を行う前に
薬理学的除細動でも、同期電気ショックによる除細動でも、48時間以上AFが続いている、または、発症時期がわからないものは塞栓症のリスクを有する。塞栓症を予防するため緊急性がない場合は、除細動を行う前に以下のどちらかをチェックする必要がある[1, 4]。
- 経食道心エコーで左房内に血栓がないことの確認
- 除細動前3週間以上抗凝固療法の施行されていること
5.3 リズムコントロールの方法
- 薬理学的除細動
- 同期電気ショックによる除細動
- カテーテルアブレーション
除細動の方法は、原疾患、心機能、年齢に応じて決定される。
・薬理学的除細動(抗不整脈薬)
Generalistとして用いるのはI群の抗不整脈薬のみ。代謝(腎・肝臓)、作用時間、副作用を考慮した上で用いる。Ⅰ群の抗不整脈薬は心不全、器質的心疾患がある患者には使用できない[2]。これらの患者やⅢ群の抗不整脈が必要になる場合は、重篤な副作用を認めるため投与に関して専門家へのコンサルテーションが必要[7]。集中治療領域では、Mgの点滴静注も推奨されている[8]。
・同期電気ショックによる除細動
頻脈性AFによる不安定化を認める緊急時にも行うが、安定している例では患者の希望、抗不整脈薬の副作用が大きい場合、薬理学的除細動が困難な場合などに検討する[1]。施行時は鎮静等が必要[4]。
・カテーテルアブレーション
カテーテルアブレーションにより、心機能が改善、虚血性脳卒中発症率や死亡率が減少したという報告もあり、カテーテルアブレーションによる洞調律の維持が有効な症例も存在する[4, 9]。
著明な左房拡大(左房前後径50 mm以上)、持続時間が長い場合(1から2年以上)では、除細動の成功率が低いことから、Learning Point 1から4の治療を優先し、基礎疾患の治療・脳梗塞予防・レートコントロールに努める[1, 9]。
今まで精査されていないAFであれば、除細動の適応も含めて、一度は専門医にコンサルテーションした方が良いと筆者は考える。
AFを見たときのマネジメントに関して解説したが、Learning Point 0 ~ 5 のSTEP を順番に評価することで、緊急同期電気ショックが必要な重症患者から内科外来に訪れる軽症な患者まで系統立てて評価が可能である。より緊急性が高く重要な順番に評価・治療介入が可能である。AFの発症には基礎疾患が影響するだけでなく,基礎疾患の治療により生命予後を改善させることができる。そのため,AF の治療だけでなく、基礎疾患の精査や治療など日々の内科管理が重要である.
① Reference
[1] 井上博. 心房細動治療(薬物)ガイドライン(2013年改訂版). 2013.
[2] January CT, Wann LS, Alpert JS, Calkins H, Cigarroa JE, Cleveland JC, Jr., et al. 2014 AHA/ACC/HRS guideline for the management of patients with atrial fibrillation: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines and the Heart Rhythm Society. J Am Coll Cardiol. 2014;64:e1-76.
[3] Toyoda K, Yasaka M, Uchiyama S, Nagao T, Gotoh J, Nagata K, et al. Blood pressure levels and bleeding events during antithrombotic therapy: the Bleeding with Antithrombotic Therapy (BAT) Study. Stroke. 2010;41:1440-4.
[4] Kirchhof P, Benussi S, Kotecha D, Ahlsson A, Atar D, Casadei B, et al. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur Heart J. 2016;37:2893-962.
[5] American Heart A, 日本Acls協会, 日本循環器学会. ACLS EPマニュアル・リソーステキスト: [バイオメディスインターナショナル]; 2014.
[6] Kirchhof P, Breithardt G, Aliot E, Al Khatib S, Apostolakis S, Auricchio A, et al. Personalized management of atrial fibrillation: Proceedings from the fourth Atrial Fibrillation competence NETwork/European Heart Rhythm Association consensus conference. Europace. 2013;15:1540-56.
[7] 山下 武. Revolution心房細動に出会ったら: メディカルサイエンス社; 2011.
[8] Bosch NA, Cimini J, Walkey AJ. Atrial Fibrillation in the ICU. Chest. 2018;154:1424-34.
[9] 赤尾 昌. これが伏見流!心房細動の診かた、全力でわかりやすく教えます。: 羊土社; 2017.
② 著者名
聖マリアンナ医科大学横浜市西部病院救命救急センター吉田 稔/吉田 徹/北野 夕佳